A 3D bionyomtatás egy rendkívül fejlett gyártási platform, amellyel szöveteket lehet nyomtatni sejtekből és végső soron létfontosságú szervekből.Ez új világokat nyithat meg az orvostudományban, miközben közvetlen hasznot hoz a szervpótlásra szoruló betegek számára.
Ahelyett, hogy megfelelő donorra várnának, vagy azt kockáztatnák, hogy a szervezet kilöki az átültetett szervet, a betegek egy erre a célra kialakított, egyedi szervet kapnak a hibás szerv pótlására.Azonban még a 3D-s bionyomtatásban az elmúlt 20 évben elért fejlődés ellenére sem történt jelentős előrelépés a komplex 3D-s biomimetikus szövetkonstrukciók előállításához.
A Szingapúri Műszaki és Tervezői Egyetem (SUTD), a Nanyang Műszaki Egyetem (NTU) és az Ázsia Egyetem kutatói szerint különösen a szövettenyésztési technológiákat kell felgyorsítani annak érdekében, hogy felszámolják a szűk keresztmetszetet a bionyomtatott többsejtű 3D szövetkonstrukciók funkcionális szövetekké történő érlelésében.A „Nyomtass nekem egy orgonát!Miért nem jelentünk még meg?”az Advances in Polymer Science című folyóiratban jelent meg.
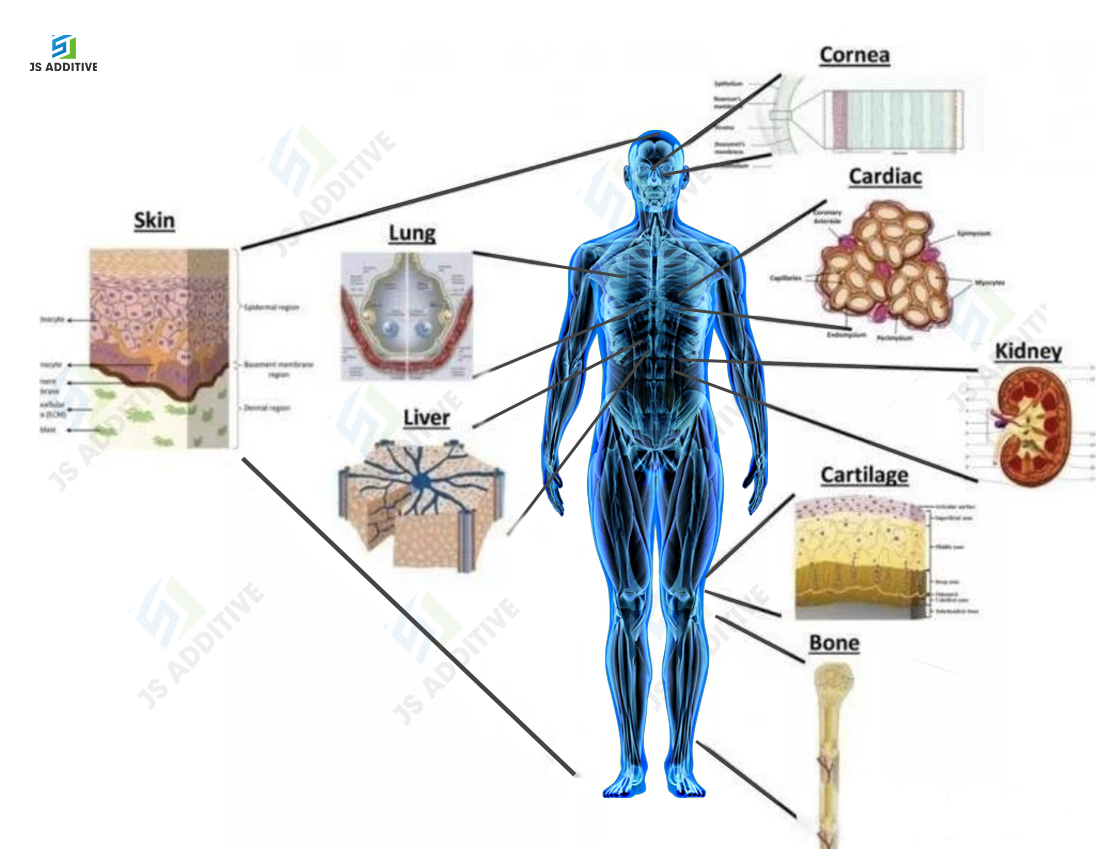
Ebben a cikkben a kutatók mélyreható áttekintést adnak a legújabb fejlesztésekről és elemzik a bionyomtatási technológiákat. A biotinta fejlesztésében, az új bionyomtatási és a szövetérési stratégiák megvalósításában elért eredményeket is elemzik.Különös figyelmet fordítanak a polimertudomány szerepére, és arra, hogy az hogyan egészíti ki a 3D bionyomtatást a szervnyomtatás néhány fő akadályának leküzdése érdekében, mint például a biomimetikus, angiogenezis és a 3D anatómiával kapcsolatos biológiai struktúrák lehetővé tétele (ahogy az alábbi képek is mutatják ).
A kiegészítő stratégiák, például a dinamikus együtttenyésztési perfúziós rendszerek alkalmazása alapvető fontosságú a bionyomtatott szövetkonstrukciók érésének és összeállításának biztosításához.Annak ellenére, hogy ma már lehetséges olyan emberi léptékű szöveteket vagy szerveket előállítani, amelyek érlelődő és részben működőképes szövetekké érhetnek, az ipar még mindig le van maradva az emberspecifikus szövetek vagy szervek bionyomtatásában a szövetspecifikus extracelluláris mátrix összetettsége miatt. ECM) és a szövetek érési folyamata – több sejttípus támogatásához megfelelő kotenyésztési táptalaj hiánya, és további szövetkondicionálás szükséges a beültetés előtt.
„Bár a 3D-s bionyomtatás még csak a kezdeti szakaszában jár, az elmúlt években elért figyelemre méltó ugrások a laboratóriumban termesztett funkcionális szervek végső valóságát sugallják.Ahhoz azonban, hogy az orvostudomány határait átléphessük, le kell küzdenünk a szövetgyártás technikai kihívásait.A specifikus biotinták nem optimalizálják a szövetek érési folyamatát.Ez végső soron óriási hatással lesz a betegek életére, akik közül sokan a 3D bionyomtatás jövőjétől függhetnek” – mondta Chua Chee Kai professzor, a tanulmány vezető szerzője.
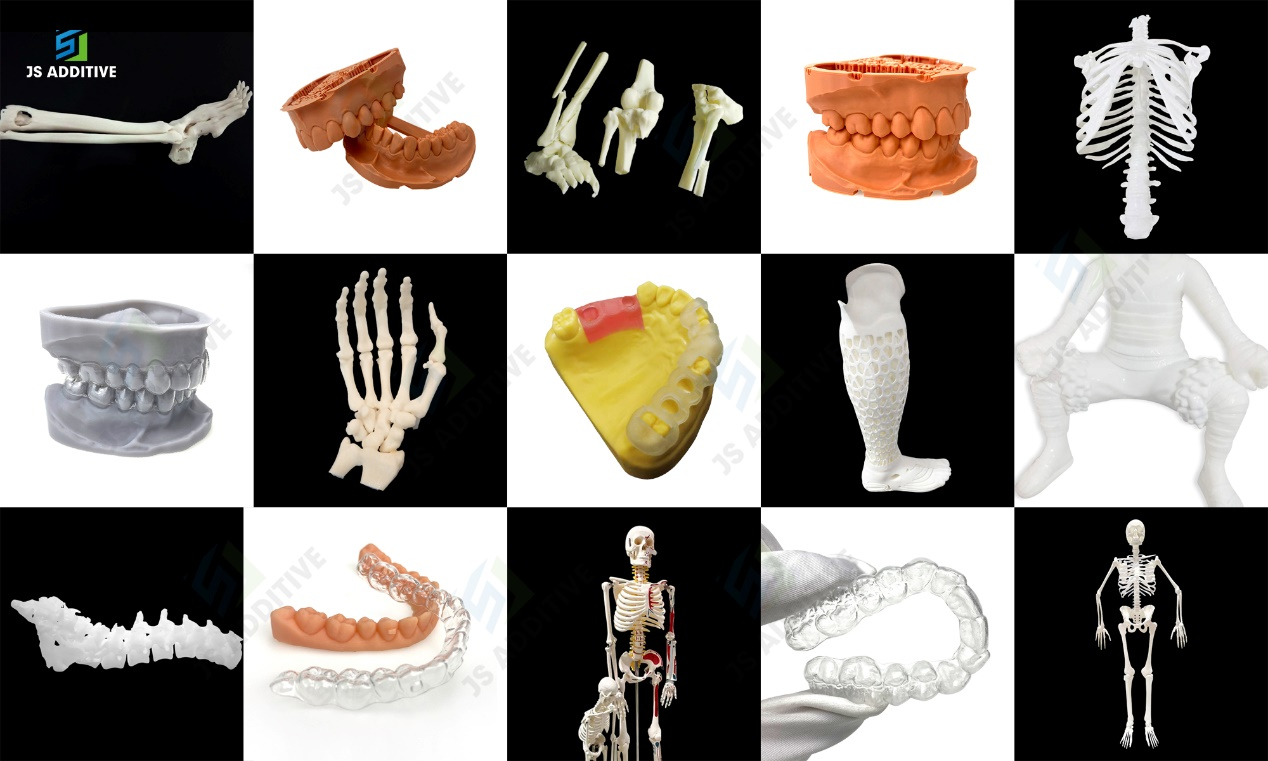
JS adalékA 3D nyomtatási szolgáltatás is folyamatosan fejlődik és fejlődik, amely az orvosi iparban egyre fejlettebb szintet ér el, hogy megfeleljen a nagyobb betegek és a tudományos kutatás igényeinek.3D nyomtatott orvosi modelljeinket és késztermékeinket széles körben használják tengerentúli alkalmazásokban is.Üdvözöljük és használjuk.